UDI für Medizinprodukte gemäß MDR
Die wichtigsten Grundlagen kompakt und verständlich
Gesetzliche Anforderungen sicher umsetzen
Medizinprodukte müssen gemäß den Anforderungen der MDR künftig eine eindeutige Produktkennung tragen. Die Kennzeichnung von Produkten mit einem maschinenlesbaren Code und den zugehörigen Daten in Eudamed (UDI-Datenbank) soll die Rückverfolgbarkeit gewährleisten und somit die Patientensicherheit erhöhen.
UDI Anforderungen werden seit Geltungsbeginn der MDR nicht nur für Hersteller von Medizinprodukten in der EU verpflichtend. Auch andere Länder übernehmen UDI Anforderungen in ihre Gesetzgebung. Die USA (FDA) gilt als Vorreiter für die Umsetzung von UDI-Vorschriften.
3-4 Stunden
Einstieg jederzeit
Teilnahmebesch.
229,00 EUR
In eigenem Tempo
Neue Kenntnisse erwerben
Zielgruppe: Hersteller von Produkten, die in den Geltungsbereich der Medizinprodukte-Verordnung (MDR) fallen.
Voraussetzungen: keine
Kursart: Online-Selbstlern-Kurs
Erwerben Sie die erforderliche Qualifikation mit Trautmann Schulungen.
Inhalte und Ablauf
Aufbau des Kurses
1. Modul: Eudamed
Das erste Modul beginnt mit einem Überblick zu den Modulen der Europäischen Datenbank für Medizinprodukte (Eudamed) und der von der EU-Kommission veröffentlichten Timeline. Es werden die Themen Vergabe der Single Registration Number (SRN) im Zusammenhang mit der Registrierung von Wirtschaftsakteuren sowie die Registrierung von Produkten behandelt.
2. Modul: UDI-System
Erfahren Sie mehr zu den Zielen des UDI-Systems und den Anforderungen der Medizinprodukte-Verordnung (MDR). Im Fokus stehen die Bausteine des UDI-Systems (UDI, UDI-Datenbank, UDI-Träger) sowie die Unterschiede von UDI-DI und UDI-PI.
3. Modul: UDI-Träger
Das Modul behandelt neben den erforderlichen Begriffsbestimmungen, die Fristen für die Umsetzung der UDI-Kennzeichnung. Erlernen Sie Anforderungen und Besonderheiten im Kontext der UDI-Träger und erfahren Sie mehr zu den Besonderheiten und Regeln für bestimmte Produktarten. Das Modul endet mit einem Überblick zu den UDI Besonderheiten für Software als Medizinprodukt.
4. Modul: Basis-UDI-DI
Die Basis-UDI-DI ist eine Besonderheit im europäischen Medizinprodukterecht. Das Modul thematisiert sowohl die europäische Umsetzung als auch den aktuellen Stand der weltweiten Implementierung der UDI. Am Beispiel des GS1 Standards erfahren Sie mehr zu den erforderlichen Schritten für Sie als Hersteller von Medizinprodukten.
Lebendiger Methodenmix mit konkreten Beispielen
Auszug aus den Schulungsunterlagen

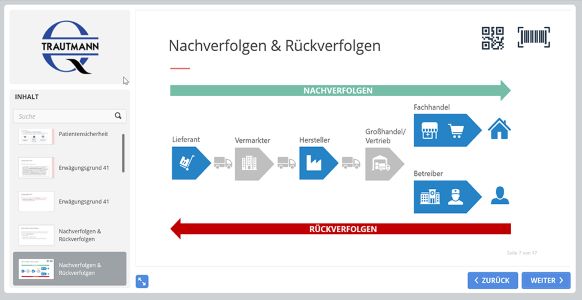
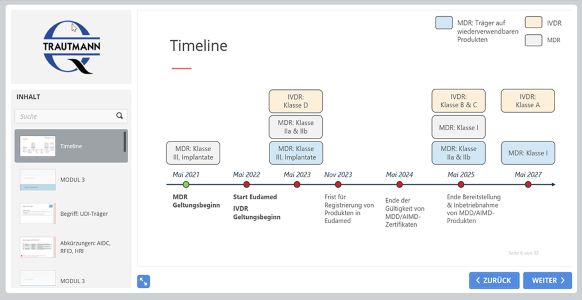

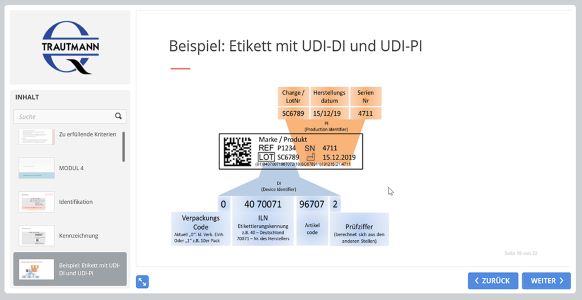

Das sagen unsere Kunden
Stimmen unserer Kurs-Teilnehmer
Flexibilität beim Lernen
Online-Seminar
Dieser Online-Kurs bietet Ihnen einen kurzen Überblick über die neuen regulatorischen Anforderungen der MDR für Medizinprodukte-UDI (Unique Device Identification). Am Ende der Schulung erhalten Sie eine Teilnahmebescheinigung „UDI für Medizinprodukteanforderungen gemäß Verordnung (EU) 2017/745“.
Hersteller von Medizinprodukten müssen die geltenden Anforderungen vollständig berücksichtigen und umsetzen. Es werden qualitativ hochwertige Schulungsunterlagen aus technischer und pädagogischer Sicht erstellt und zusammengestellt. Diese Inhalte wurden in Zusammenarbeit mit erfahrenen Auditoren aus der Gesundheitsbranche erstellt, um Ihnen das notwendige Wissen leicht verständlich zu vermitteln.
Mit unseren Online-Schulungen bieten wir Ihnen Flexibilität für die Weiterbildung. Sie können in Ihrem eigenen Tempo fortfahren und das Training jederzeit beenden. Dadurch sind Sie vollkommen orts- und zeitunabhängig.
Stellen Sie Ihre Buchungsanfrage über unser Kontaktformular oder buchen Sie den Kurs direkt per PayPal.
Einfache und schnelle Anmeldung zum Online Kurs
Formular
-
1. Formular ausfüllen und zurücksenden
-
2. Rechnungsbetrag überweisen
-
3. Freischaltung und Erhalt der Zugangsdaten
-
4. Kurs starten
Direkt buchen
-
1. Ein kostenloses Kundenkonto erstellen
-
2. Gewünschten Kurs auswählen
-
3. Teilnahmegebühr mit PayPal bezahlen
-
4. Kurs starten
Angebot
-
Sonderkonditionen ab 10 Teilnehmern
-
Sparen mit dem Abo-Modell
-
Eigene Lernplattform für Unternehmen
-
Individuelle Kurse
Häufig gestellte Fragen (FAQ)
In unserem zentralem Bereich Häufig gestellte Fragen (FAQ) finden Sie alle Antworten und die häufigsten Fragen zu Ihrem Thema.
Haben Sie Fragen?
Sie interessieren sich für eine Beratung oder eine Schulung und möchten sich dafür mit uns in Verbindung setzen?
Vereinbaren Sie gerne einen Termin für ein Gespräch : Kostenlos und unverbindlich.
Beratung: +49 34293 4797-20
Schulungen: +49 34293 4797-27

