Schulung Technische Dokumentation
Kompaktes Format, ideal für Berufstätige
Durch Wissen auf der sicheren Seite sein

Die technische Dokumentation ist wesentlicher Bestandteil des Konformitätsbewertungsverfahrens für Medizinprodukte. Als zentrale Nachweisdokumentation ist sie Voraussetzung für die Zulassung von Medizinprodukten. Seit dem Geltungsbeginn der europäischen Medizinprodukte-Verordnung werden die Hersteller in der Phase nach dem Inverkehrbringen stärker in die Verantwortung genommen.
Diese müssen die geltenden Bestimmungen mit der gebührenden Sorgfalt berücksichtigen und Ihre Pflichten gemäß Artikel 10 MDR wahrnehmen. Anhang II und Anhang III der Verordnung (EU) 2017/745 beschreiben die Anforderungen und Bestandteile der technischen Dokumentation ausführlich und detailliert. Informationen über Erfahrungen mit ihren Produkten müssen systematisch und aktiv zusammengetragen werden, um die technische Dokumentation (u.a. Dokumente zu Risikobewertung, klinische Bewertung) auf dem neuesten Stand zu halten.
Diese Online-Schulung vermittelt kompakt und verständlich das für die technische Dokumentation notwendige Wissen und Methoden.
3-4 Stunden
Einstieg jederzeit
Teilnahmebesch.
229,00 EUR
Schritt für Schritt, mit Ihrer eigenen Zeitplanung
Erforderliche Qualifikation erwerben
Zielgruppe:
Bevollmächtigte, Hersteller und Vertriebsunternehmen der Medizinproduktebranche
Voraussetzungen: keine
Kursart: Online-Selbstlern-Kurs
Erwerben Sie die erforderliche Qualifikation mit Trautmann Schulungen.
Inhalte und Ablauf
Aufbau des Kurses
Die Schulung zur Technischen Dokumentation umfasst folgende Themen:
1. Modul: Medizinprodukte-Verordnung
Das erste Modul beginnt mit einem Überblick zur neuen europäischen Medizinprodukte-Verordnung und behandelt die Fristen zur Umsetzung. Es werden Inhalt und Systematik der Verordnung thematisiert und neue bzw. erweiterte Anforderungen beleuchtet. Am Ende der Lerneinheit werden Ihnen die MDCG Guidance Dokumente kurz vorgestellt.
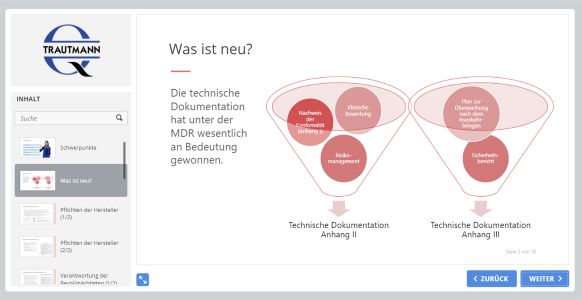
2. Modul: Was ist neu?
In diesem Modul werden die Pflichten der Hersteller nach Artikel 10 MDR und die Verantwortung der Bevollmächtigten dargestellt. Sie lernen die Anforderungen an die technische Dokumentation kennen und erfahren wer für die Aktualisierung der Nachweisdokumentation verantwortlich ist. Abschließend werden die grundlegenden Sicherheits- und Leistungsanforderungen gemäß Anhang I der Medizinprodukte-Verordnung benannt und die Bedeutung der technischen Dokumentation im Konformitätsbewertungsverfahren beleuchtet.
3. Modul: Gap-Analyse für Bestandsprodukte
Lernen Sie eine Herangehensweise zur Anpassung der technischen Dokumentation Ihrer Bestandsprodukte kennen, in dem Sie relevante Begriffe unterscheiden können, die Ihnen helfen Ihre Produkte richtig zu identifizieren. Im Fokus stehen die Zweckbestimmung und die Produktbeschreibung auf deren Grundlage die Zuordnung zu einer Risikoklasse erfolgt. Ermitteln Sie im Anschluss die zutreffenden grundlegenden Sicherheits- und Leistungsanforderungen Ihrer Produkte. Das Modul endet mit einer Handlungsempfehlung.
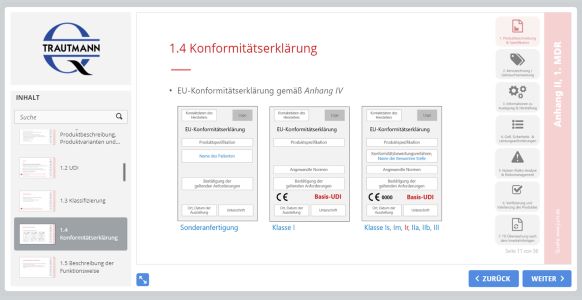
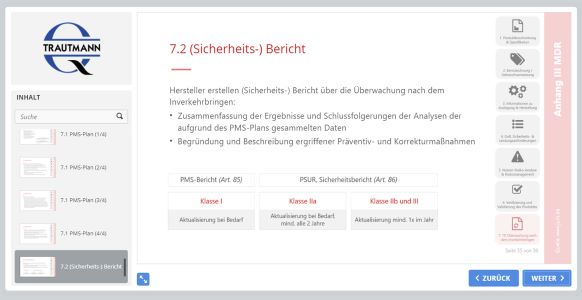
4. Modul: Struktur der technischen Dokumentation
Das vierte Modul behandelt die bekanntesten Strukturmodelle der technischen Dokumentation, z. B. STED (Summary Technical Documentation) und erläutert im Anschluss die Bestandteile der technischen Dokumentation gemäß Anhang II und Anhang III der MDR. Darüber hinaus werden die Gliederungspunkte der technischen Dokumentation Schritt für Schritt erläutert und einzureichende Dokumente benannt. Das Training verdeutlicht die Bedeutung der Dokumentenlenkung zur Erfüllung der umfassenden Anforderungen der Medizinprodukte-Verordnung.
Lebendiger Methodenmix mit konkreten Beispielen
Auszug aus den Schulungsunterlagen



Das sagen unsere Kunden
Stimmen unserer Kurs-Teilnehmer
Flexibilität beim Lernen
Online-Seminar
Der Online-Kurs „Technische Dokumentation für Medizinprodukte“ setzt keine speziellen Kenntnisse voraus. Die relevanten Grundlagen werden im Rahmen der Schulung vermittelt. Die Lernmodule eignen sich gleichermaßen für Anfänger und Fortgeschrittene.
Unsere Schulungsunterlagen werden in Zusammenarbeit mit Experten der Gesundheits- und Medizinbranche erarbeitet, um Ihnen fachliches Wissen übermitteln zu können. Alle Schulungen bieten Ihnen Flexibilität für Ihre individuelle Weiterbildung durch Fortschritt im eigenen Lerntempo. Da Sie die einzelnen Mdoule jederzeit pausieren können, sind Sie dementsprechend unabhängig von Ort und Zeit und können optimale Ergenisse erzielen.
Stellen Sie Ihre Buchungsanfrage über unser Kontaktformular oder buchen Sie den Kurs direkt per PayPal.
Einfache und schnelle Anmeldung zum Online Kurs
Formular
-
1. Formular ausfüllen und zurücksenden
-
2. Rechnungsbetrag überweisen
-
3. Freischaltung und Erhalt der Zugangsdaten
-
4. Kurs starten
Direkt buchen
-
1. Ein kostenloses Kundenkonto erstellen
-
2. Gewünschten Kurs auswählen
-
3. Teilnahmegebühr mit PayPal bezahlen
-
4. Kurs starten
Angebot
-
Sonderkonditionen ab 10 Teilnehmern
-
Sparen mit dem Abo-Modell
-
Eigene Lernplattform für Unternehmen
-
Individuelle Kurse
Häufig gestellte Fragen (FAQ)
In unserem zentralem Bereich Häufig gestellte Fragen (FAQ) finden Sie alle Antworten und die häufigsten Fragen zu Ihrem Thema.
Haben Sie Fragen?
Sie interessieren sich für eine Beratung oder eine Schulung und möchten sich dafür mit uns in Verbindung setzen?
Vereinbaren Sie gerne einen Termin für ein Gespräch : Kostenlos und unverbindlich.
Beratung: +49 34293 4797-20
Schulungen: +49 34293 4797-27

